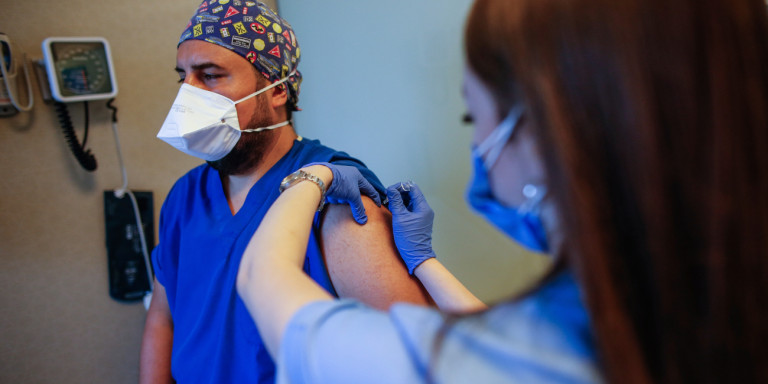
Με την πανδημία του κορωνοϊού να καλπάζει ανά την υφήλιο επιστήμονες και φαρμακευτικοί κολοσσοί εργάζονται πυρετωδώς για την ανάπτυξη των εμβολίων που θα ανάψουν το πράσινο φως για τη σταδιακή επιστροφή στην κανονικότητα.
Δεκάδες εμβόλια αναπτύσσονται και δοκιμάζονται σ’ ολόκληρο τον κόσμο και το τελευταίο διάστημα ανακοινώθηκαν ελπιδοφόρα νέα για κάποια εξ’ αυτών, όπως π.χ. χθες για εκείνο των AstraZeneca/Πανεπιστημίου της Οξφόρδης, τα αποτελέσματα της δεύτερης φάσης των κλινικών δοκιμών του οποίου έδειξαν ότι παράγει ισχυρή ανοσοαπόκριση σε υγιείς ηλικιωμένους. Η λίστα που ακολουθεί περιλαμβάνει εκείνα που προηγούνται αυτή τη στιγμή στην κούρσα και πότε μπορεί να κυκλοφορήσουν στην αγορά. Πιο μπροστά βρίσκονται τα εμβόλια της Pfizer και της Μοderna, με την Pfizer, μάλιστα, σήμερα να καταθέτει αίτημα έγκρισης στην αμερικανική FDA.
Pfizer – BioNTech
Το εμβόλιο του αμερικανικού φαρμακευτικού κολοσσού Pfizer και της γερμανικής εταιρείας βιοτεχνολογίας BioNTech βρίσκεται στην τρίτη φάση των κλινικών δοκιμών κι όπως διαπιστώθηκε ήταν κατά 95% αποτελεσματικόστην πρόληψη της μόλυνσης των εθελοντών από το φονικό κορωνοϊό. Σύμφωνα με τη Pfizer η αποτελεσματικότητα του ΒNT162b2, όπως αποκαλείται το εμβόλιό της, ήταν η ίδια σε όλες τις ηλικιακές ομάδες ανεξαρτήτου φυλής και εθνικής προέλευσης και δεν διαπιστώθηκαν σοβαρές παρενέργειες. Η αποτελεσματικότητα άγγιξε ποσοστό άνω του 94% σε άτομα ηλικίας άνω των 65 ετών.
Η τελική ανάλυση δόθηκε στη δημοσιότητα μία εβδομάδα μετά την ανακοίνωση των ενδιάμεσων αποτελεσμάτων που έδειξαν αποτελεσματικότητα του εμβολίου σε ποσοστό άνω του 90%. Η Φάση 3 των κλινικών δοκιμών του εμβολίου ξεκίνησε στις 27 Ιουλίου με τη συμμετοχή 43.661 εθελοντών, εκ των οποίων οι 41.135 έλαβαν δεύτερη δόση ή εικονικό φάρμακο. Σύμφωνα με τον διευθύνοντα σύμβουλο της BioNTech, Ουγκούρ Σαχίν η εταιρεία του και η Pfizer θα ζητήσουν σήμερα (Παρασκευή) από τον αμερικανικό Οργανισμό Τροφίμων και Φαρμάκων άδεια επείγουσας χρήσης του εμβολίου. Σχολιάζοντας πόσο γρήγορα μπορεί να γίνει η αξιολόγηση της αίτησης από την αρμόδια επιτροπή του FDA είπε ότι «μπορεί να δοθεί έγκριση ή κατά περίπτωση αδειοδότηση εντός του 2020, πράγμα που θα βοηθήσει να ξεκινήσουμε την αποστολή των πρώτων δόσεων πριν το τέλος της χρονιάς», αποφεύγοντας ωστόσο χρονικά να καθορίσει πόσο θα διαρκέσει η διαδικασία για να εκδοθεί η απόφαση του ρυθμιστικού φορέα. Θα ακολουθήσει εντός ολίγων ημερών η αίτηση έγκρισης του εμβολίου στις αντίστοιες ευρωπαϊκές αρχές.
Την ίδια ώρα προχωρά με πυρετώδεις ρυθμούς η παραγωγή του εμβολίου στο Βέλγιο, αλλά και τις ΗΠΑ. Ηδη υπάρχουν 20.000 εκατ. δόσεις του εμβολίου έτοιμες. Ο Ελληνας CEO της Pfizer Αλβέρτος Μπουρλά, σε συνέντευξή του χθες ανέφερε ότι οι αιτήσεις για έγκριση του εμβολίου θα κατατεθούν τις επόμενες ημέρες και η διανομή του εμβολίου θα αρχίσει ώρες αφότου λάβει την έγκριση.
Μoderna
H αμερικανική φαρμακευτική εταιρεία Moderna χρησιμοποιεί παρόμοια τεχνολογία με εκείνη της Pfizer για το εμβόλιό της. Το mRNA-1273, όπως αποκαλείται, βρίσκεται επίσης στην 3η Φάση των κλινικών δοκιμών, στις οποίες συμμετέχουν 30.000 εθελοντές στις ΗΠΑ. Η Moderna ανακοίνωσε προ ημερών ότι το εμβόλιό της είναι αποτελεσματικό κατά 94,5%. Tο εμβόλιο των δύο δόσεων της Moderna εγχέει στο σώμα γενετικό υλικό, που ονομάζεται mRNA , το οποίο χρησιμοποιούν στη συνέχεια τα κύτταρα για να μιμηθούν την πρωτεϊνη ακίδα, που χρησιμοποιεί ο κορωνοϊός για να εισβάλει σ’ αυτά. Η πρωτεΐνη ακίδα καλύπτει την επιφάνεια του ιού και είναι ένας από τους κύριους στόχους της ανοσολογικής απόκρισης του σώματος για την εξάλειψη της λοίμωξης. Τα ενδιάμεσα αποτελέσματα, που ανακοινώθηκαν τη Δευτέρα, βασίζονται σε ανάλυση επιβεβαιωμένων κρουσμάτων της Covid-19 μεταξύ των εθελοντών που έλαβαν εικονικά φάρμακα και εκείνων που έλαβαν το εμβόλιο, ξεκινώντας δύο εβδομάδες μετά τη χορήγηση της δεύτερης δόσης.
Το εμβόλιο της Moderna δεν αναμένεται να είναι διαθέσιμο εκτός των ΗΠΑ έως το επόμενο έτος. Η εταιρεία δήλωσε ότι θα έχει 20 εκατομμύρια δόσεις έτοιμες να αποσταλούν στις ΗΠΑ πριν από το τέλος του 2020 και ελπίζει να παρασκευάσει από 500 εκατομμύρια έως ένα δισεκατομμύριο δόσεις παγκοσμίως τον επόμενο χρόνο, ενώ φουλάρει τις μηχανές της σε συνεργασία με την ελβετική Lonza Group AG για την εκκίνηση της ευρωπαϊκής παραγωγής μέχρι το τέλος του μήνα, που σημαίνει ότι θα είναι διαθέσιμο το νωρίτερο την ερχόμενη άνοιξη.
AstraZeneca – Πανεπιστήμιο της Οξφόρδης
To εμβόλιο που αναπτύσσουν το Πανεπιστήμιο της Οξφόρδης και η AstraZeneca θεωρείτο αρχικά ότι ηγείτο της κούρσας και τώρα βρίσκεται λίγες εβδομάδες πίσω από την Pfizer. Η βασικότερη διαφορά του ChAdOx1 nCoV-19 σε σχέση με εκείνo της Pfizer έγκειται στο ότι βασίζεται σε έναν «απενεργοποιημένο» αδενοϊό, που προκαλεί κρυολόγημα και εντοπίζεται στους χιμπατζήδες. Στον συγκεκριμένο αδενοϊό, ωστόσο, οι επιστήμονες της Οξφόρδης πρόσθεσαν γενετικές οδηγίες για την πρωτεΐνη ακίδα που χρησιμοποιεί ο νέος κορωνοϊός για να να προσβάλει τον ανθρώπινο οργανισμό, πράγμα που σημαίνει ότι το εμβόλιο της Οξφόρδης και της AstraZeneca «διδάσκει» το ανοσοποιητικό σύστημα να αναγνωρίζει τον SARS-CoV-2 και να δημιουργεί ανοσολογική αντίδραση.
Τα αποτελέσματα από τις δοκιμές τελικού σταδίου του υποψήφιου εμβολίου του Πανεπιστημίου της Οξφόρδης κατά της covid-19 θα έχουν «οπωσδήποτε» γίνει γνωστά πριν από τα Χριστούγεννα, δήλωσε σήμερα ο επικεφαλής των ερευνητών για τις δοκιμές, προσθέτοντας ότι ακόμη είναι πολύ νωρίς για να γνωρίζουμε την αποτελεσματικότητά του αν και δήλωσε πολύ ικανοποιημένος από τα αποτελέσματα που δόθηκαν νωρίτερα σήμερα στη δημοσιότητα και τα οποία έδειξαν εξαιρετικά καλή ανοχή στο εμβόλιο σε άτομα ηλικίας άνω των 55. Πάντως έχουν ήδη παρασκευαστεί στην Ινδία 40 εκατ. δόσεις του συγκεκριμένου εμβολίου.
CanSino-Ινστιτούτο Βιοτεχνολογίας Πεκίνου
Το Ad5-nCoV της CanSino είναι ένα εμβόλιο ιικού φορέα και ένα από εκείνα που ηγούνται στην κούρσα στην Κίνα. Τα αποτελέσματα της Β΄Φάσης των κλινικών δοκιμών έδειξαν ότι το εμβόλιο αυτό παράγει «σημαντική ανοσοαπόκριση στην πλειονότητα όσων το έχουν λάβει, χωρίς σοβαρές παρενέργειες». Όπως και εκείνο των AstraZeneca/Πανεπιστημίου της Οξφόρδης το εμβόλιο αυτό χρησιμοποιεί έναν ιό, που αποκαλείται αδενοϊός, προκειμένου να μεταφέρει γενετικό υλικό από την πρωτεΐνη του νέου κορωνοϊού στο ανθρώπινο σώμα. Aν και από τεχνικής άποψης βρίσκεται ακόμη στη δεύτερη φάση των δοκιμών, τον περασμένο Ιούνιο η CanSino – μεγαλύτερος μέτοχος της οποίας είναι ο αμερικανικός φαρμακευτικός κολοσσός Elli Lilly, σύμφωνα με τη Refinitiv data – έγινε η πρώτη φαρμακευτική εταιρεία που έλαβε άδεια για περιορισμένη χρήση του εμβολίου της σε ανθρώπους και συγκεκριμένα για μέλη των ενόπλων δυνάμεων της Κίνας. Ωστόσο, παραμένει άγνωστο, πότε θα διατεθεί στο κοινό.
Sputnik V
Το Sputnik V, το εμβόλιο κατά του κορωνοϊού που ηγείται της κούρσας στη Ρωσία, χρησιμοποιεί δύο στελέχη αδενοϊού και απαιτεί και δεύτερη δόση μετά από 21 ημέρες για ενίσχυση της ανοσοαπόκρισης. Αν και δεν έχουν ακόμη δημοσιευτεί στοιχεία για την ασφάλειά του εμβολίου, το κρατικό ταμείο πλούτου της χώρας υποστηρίζει ότι το Sputnik V είναι κατά 92% αποτελεσματικό.
Προς το παρόν, όπως επεσήμανε προ ημερών και ο Ηλίας Μόσιαλος, οι κλινικές δοκιμές του εμβολίου Sputnik V Phase III έχουν εγκριθεί και βρίσκονται σε εξέλιξη στη Λευκορωσία, τα ΗΑΕ, τη Βενεζουέλα και άλλες χώρες, καθώς και η Φάση II-III στην Ινδία.
Johnson & Johnson
Η Johnson & Johnson έχει ήδη ξεκινήσει από τον Σεπτέμβριο την τρίτη φάση των κλινικών δοκιμών του εμβολίου της με τη συμμετοχή 60.000 εθελοντών στις ΗΠΑ, την Αργεντινή, τη Βραζιλία, τη Χιλή, την Κολομβία, το Μεξικό, το Περού και τη Νότια Αφρική, χώρες στις οποίες προστέθηκε από χθες και η Βρετανία.
Το Ad26.COV2-S χρησιμοποιεί έναν αδενοϊό, προκειμένου να μεταφέρει την ανοσοποιητική πρωτεΐνη στο σώμα, ενώ η Johnson & Johnson εξετάζει ξεχωριστά ένα εμβόλιο ενάντια στον SARS-CoV-2, το οποίο δυνητικά θα μπορεί να είναι αποτελεσματικό με μία δόση.
Novavax
Το εμβόλιο που ανέπτυξε η αμερικανική εταιρεία βιοτεχνολογίας Novavax με έδρα το Μέριλαντ χορηγείται σε δύο δόσεις με διαφορά 21 ημερών. Στα τέλη Σεπτεμβρίου ξεκίνησε στη Βρετανία η τελική φάση των δοκιμών του με τον εμβολιασμό 10.000 ανθρώπων ηλικίας 18 ως 84 ετών, ενώ προ ημερών ο αμερικανικός Οργανισμός Τροφίμων και Φαρμάκων (FDA) άναψε το πράσινο φως για την επιτάχυνση των κλινικών ερευνών του NVX-CoV2373 με τη διαδικασία του «fast track» (δηλαδή επιτάχυνση των ερευνών με περισσότερους εθελοντές) στις ΗΠΑ.